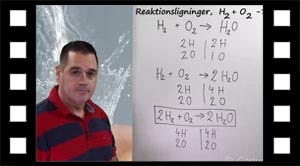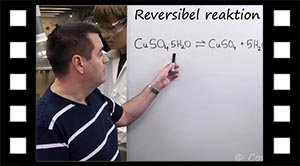Indholdsfortegnelse
12.1.1 Kemiske reaktionsligninger
En kemisk reaktion er, når kemiske forbindelser omdannes til andre kemiske forbindelser.
Kemiske reaktioner kan skrives lidt som en ligning i matematik, men i stedet for et lighedstegn bruger man en reaktionspil.
I matematik betyder et lighedstegn, at det, der står på venstresiden, er det samme som på højresiden.
På samme måde skal det, der står på venstresiden af en reaktionspil, være det samme som på højresiden. I hvert fald i forhold til nogle bevarelses-sætninger, som skal være opfyldt i alle reaktionsligninger.

12.1.2 Afstemning af reaktionsligninger
Der skal altid være lige mange grundstofatomer på højre side som på venstre side af reaktionspilen. I det følgende afstemmes et par kemiske reaktionsligninger.
Eksempel 1:
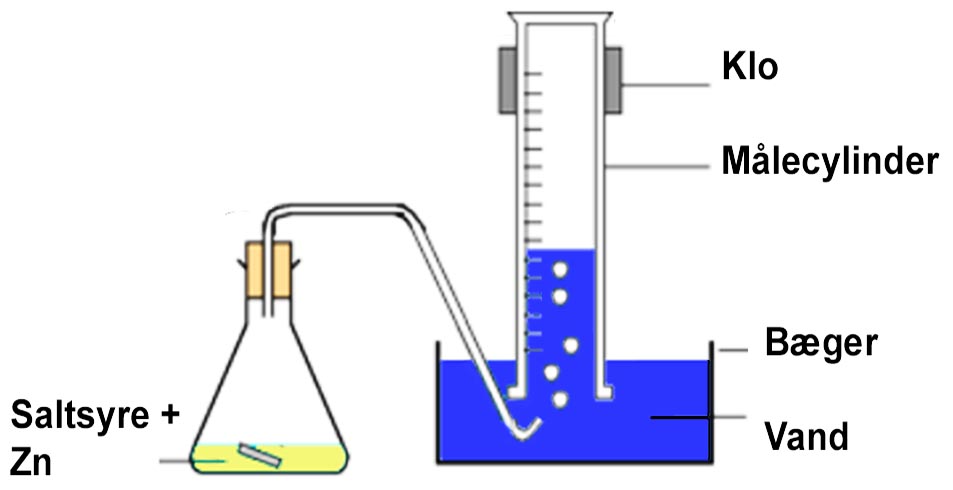
Her kan du se reaktionen foregå:
12.1.3 Fast, flydende eller gas
Når man opskriver sin reaktionsligning, har man mulighed for at tilføje de forskellige stoffers tilstandsform. Der findes tre tilstandsformer nemlig fast (solid), flydende (liquid) og gas, og de forkortes (s), (l) og (g).
12.1.4 Energi og kemiske reaktioner
Nogle reaktioner frigiver energi og andre kræver energi.
En vigtig reaktion er fotosyntese, hvor planter bruger solens energi til at opbygge molekyler, der indeholder energi – det kan være en sukkerroe. Den proces kræver altså energi.
Vi kan spise sukkerroens fructose, som vi kan forbrænde i vores krop og omsætte til energi.
I har i forsøget med brint-ballonen set, hvordan man ved afbrænding af hydrogen med oxygen får vand og en masse energi. Hvis man tilfører energi, kan man få reaktionen til at gå baglæns. Det er det, der sker i ved elektrolyse af vand.
12.1.5 Elektrolyse
Når man brænder hydrogen med oxygen, får man vand. Man kan få reaktionen til at gå den anden vej: Ved elektrolyse kan man spalte vand, H2O til H2 og O2. Denne reaktion kræver energi, som kommer fra elektrisk strøm.
12.1.6 Reversible – og irreversible reaktioner
Processen med magnesiums forbrænding til magnesiumoxid udviklede en masse energi, og magnesiumoxid har et meget lavere energi niveau end magnesium. Den reaktion kan man ikke lige få til at gå tilbage igen. Sket er sket. Det kaldes en irreversibel reaktion.
Afbrænding af hydrogen-ballonen, hvor hydrogen afbrændes med oxygen, frigives energi, men kan godt gå baglæns ved tilførsel af elektrisk energi, som I så ved elektrolyse af vand. Det kaldes en reversibel reaktion.
En reversibel reaktion er en kemisk reaktion, der kan gå begge veje. For eksempel kan kobbersulfat, der har vand bundet, afgive vandet og optage det hurtigt igen.
12.1.7 Reaktionshastighed
Atmosfærisk luft indeholder cirka 20 % Oxygen, ilt. Hvis man sætter iltkoncentrationen op, foregår forbrændingsreaktioner meget voldsommere og hurtigere.
Hvis man bygger et bål, og det har svært ved at komme i gang, kan man puste til det. Det, man i virkeligheden gør, er at tilføre ekstra ilt, så forbrændingen bedre kan foregå.
Der er flere måder at ændre reaktionshastigheder på: Man kan ændre koncentrationen af de stoffer der reagerer (kaldet reaktanterne), man kan ændre temperaturen, eller trykket.
Man kan også tilsætte en katalysator, der får reaktionen til at gå hurtigere, eller man kan tilsætte en inhibitor, der får reaktionen til at gå langsommere.